
Η αμυλοείδωση είναι μια σπάνια πολυσυστηματική νόσος, η οποία προκαλεί προοδευτική προσβολή πολλών οργάνων και σχετίζεται με αυξημένη θνητότητα. Ποσοστό >98% της καρδιακής αμυλοείδωσης οφείλεται σε ινίδια αποτελούμενα από μονοκλωνικές ελαφριές αλυσίδες ανοσοσφαιρίνης (AL) ή τρανσθυρετίνη (ATTR). Η AL αμυλοείδωση είναι το αποτέλεσμα αιματολογικής κακοήθειας και η ATTR αμυλοείδωση οφείλεται σε αλλαγές που συμβαίνουν στην πρωτεΐνη της τρανσθυρετίνης, μιας πρωτεΐνης που μεταφέρει τη θυροξίνη.1
Η ATTR είναι αποτέλεσμα είτε της γήρανσης («γεροντική» μορφή ή wild type ATTR) είτε της εμφάνισης μεταλλάξεων στο γονίδιο TTR (οικογενής μορφή, hereditary ATTR). Οι μεταλλάξεις οδηγούν στην παραγωγή μιας μη φυσιολογικής TTR πρωτεΐνης, η οποία συσσωρεύεται σε ζωτικά όργανα, συμπεριλαμβανομένων των νεύρων, της καρδιάς και του γαστρεντερικού σωλήνα. Η ATTR μπορεί να οδηγήσει σε πτωχή ποιότητα ζωής, συμπτώματα καρδιακής ανεπάρκειας και πρόωρο θάνατο.

Dr Αλέξιος Αντωνόπουλος
Ειδικός στη Μαγνητική Τομογραφία Καρδιάς, Ακαδημαϊκός Υπότροφος, ΕΚΚΑΝ, Α’ Παν. Καρδιολογική Κλινική, ΕΚΠΑ

Χαράλαμπος Βλαχόπουλος
Καθηγητής Καρδιολογίας, Υπεύθυνος του Κέντρου Κληρονομικών Παθήσεων της Α Καρδιολογική Κλινική ΕΚΠΑ
Αν και παλαιότερα πιστεύαμε πως η ATTR είναι μια σχετικά σπάνια νόσος, τα τελευταία χρόνια, με τις εξελίξεις στον τομέα των διαγνωστικών τεχνικών, έχει γίνει κατανοητό πως η TTR αμυλοείδωση είναι πολύ συχνότερη, ενδεχομένως περισσότερο και από την AL αμυλοείδωση. Σήμερα, είναι κατανοητό πως πληθυσμοί ασθενών με αυξημένο επιπολασμό ATTR είναι οι ασθενείς με υπετροφική μυοκαρδιοπάθεια και οι ασθενείς με υπερτροφία της αριστερής κοιλίας και καρδιακή ανεπάρκεια με διατηρημένο κλάσμα εξώθησης (HFpEF). Επίσης, οι ασθενείς με σοβαρού βαθμού στένωση αορτικής βαλβίδας που υποβάλλονται σε διακαθετηριακή εμφύτευση αορτικής βαλβίδας (TAVI), οι οποίοι είναι συνήθως ασθενείς με προχωρημένο μέσο όρο ηλικίας, μπορεί να κρύβουν ATTR σε ποσοστό ως και 15%. Αξίζει να σημειωθεί πως η παρουσία ATTR σχετίζεται με χειρότερη πρόγνωση μετά από TAVI.
Περάν της μυοκαρδιακής προσβολής, η αμυλοείδωση μπορεί να εκδηλωθεί και με εξωκαρδιακά ευρήματα, στα οποία άλλωστε βασίζεται εν μέρει και η διάγνωση της νόσου (red flags, Εικόνα 1). Τέτοια εξωκαρδιακά ευρήματα είναι η πολυνευροπάθεια, δερματικές αλλοιώσεις, μακρογλωσσία, σύνδρομο καρπιαίου σωλήνα, στενώσεις οσφυικής μοίρας σπονδυλικής στήλης και οφθαλμολογικές διαταραχές λόγω της εναπόθεσης του αμυλοειδούς. Η προσβολή της καρδιάς παρουσιάζεται συχνά σε πιο όψιμη φάση στη ζωή του ατόμου, με την «συγκεντρικού τύπου» (συμμετρική ή ασύμμετρη) υπερτροφία της αριστερής κοιλίας να αποτελεί την κύρια και πιο συχνή εκδήλωση.1 Σε ασθενή με υπερτροφία της αριστερής κοιλίας (≥12mm) και παρουσία ενός ή περισσοτέρων εξωκαρδιακών ευρημάτων δηλωτικών αμυλοείδωσης (red flags, βλ. ανωτέρω) θα πρέπει να γίνεται έλεγχος για αμυλοείδωση. Δυστυχώς, η νόσος δεν αναγνωρίζεται ακόμα και σήμερα όσο έγκαιρα θα μπορούσε. Είναι συνεπώς απαραίτητη η εγρήγορση των κλινικών για ευρήματα και σημεία που μπορεί να υποδηλώνουν παρουσία αμυλοείδωσης. Η διάγνωση της ATTR μπορεί να καθυστερήσει κατά μέσο όρο 5 έτη μετά την εκδήλωση του πρώτου συμπτώματος. O έλεγχος μπορεί να γίνει από εξειδικευμένο ιατρό Καρδιολόγο και Νευρολόγο, και βασίζεται σε κλινικό, βιοχημικό, απεικονιστικό και γενετικό έλεγχο.
Τα διαγνωστικά κριτήρια μπορούν να διαχωριστούν σε δύο κατηγορίες: επεμβατικά και μη επεμβατικά. Στα επεμβατικά συγκαταλέγεται η ενδομυοκαρδιακή βιοψία που αποτελεί και εξέταση εκλογής έως και σήμερα. Η ATTR προκαλεί την εξωκυτταρική εναπόθεση ινιδίων τρανσθυρετίνης στην καρδιά με την παθογνωμονική ιστολογική ιδιότητα της πράσινης απόχρωσης όταν παρατηρείται υπό πολωμένο φως μετά από χρώση με το ερυθρό του Κονγκό.
Η μη επεμβατική οδός για τη διάγνωση της ATTR (χωρίς ανάγκη ενδομυοκαρδιακής βιοψίας) βασίζεται στην παρουσία όλων των παρακάτων κριτηρίων:
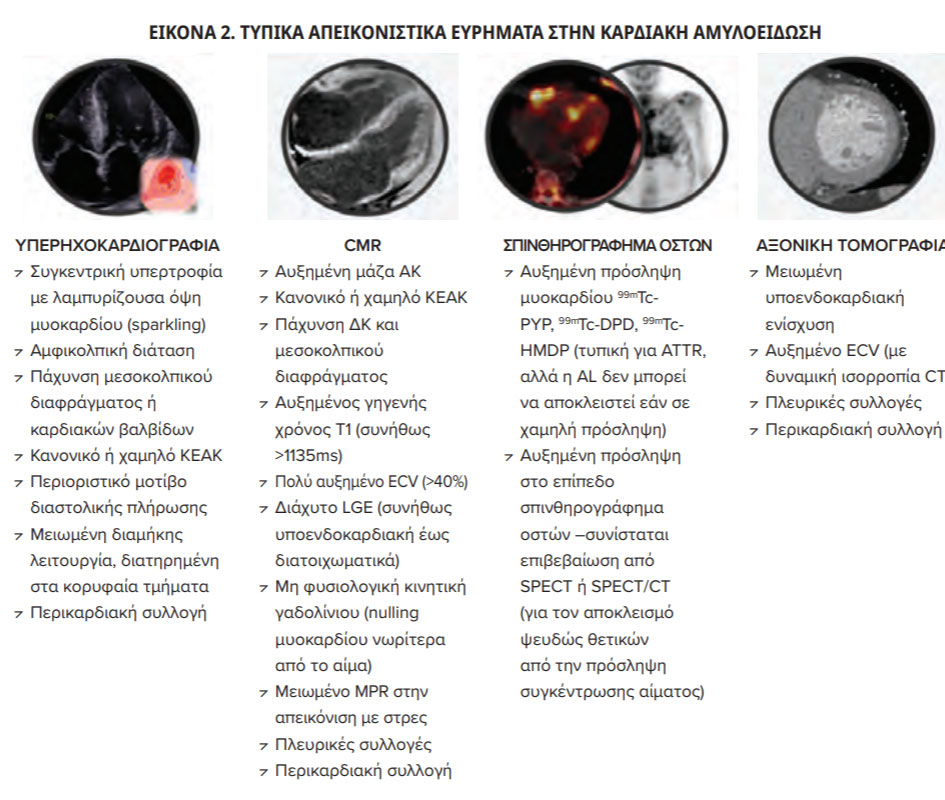
Τυπικών ευρημάτων αμυλοείδωσης στο διαθωρακικό υπερηχοκαρδιογράφημα ή/ και την μαγνητική τομογραφία καρδιάς σε συνδυασμό με β. σπινθηρογράφημα οστών (Tc99m-DPD, Tc99m-PYP ή Tc99m-HMDP) θετικό για αμυλοείδωση (Grade II ή ΙΙΙ) και γ. απουσία κλωνικής δυσκρασίας με βάση τις κ/λ ελεύθερες ελαφριές αλύσους, την ηλεκτροφόρηση κα ανοσοσοκαθήλωση πρωτεϊνών ορού και ούρων. Όταν πληρούνται όλα τα ανωτέρω κριτήρια είναι αξιόπιστη η διάγνωση της καρδιακής ATTR με μη επεμβατικό τρόπο. 3,4 Τα τυπικά απεικονιστικά ευρήματα στην καρδιακή αμυλοείδωση συνοψίζονται στην Εικόνα 2. Στο διαθωρακικό υπερηχοκαρδιογράφημα τα τυπικά ευρήματα της αμυλοείδωσης είναι η υπερτροφία της αριστερής κοιλίας με διατηρημένο κλασμα εξώθησης και περιοριστική φυσιολογία με αμφικολπική διάταση και διατηρημένη επιμήκη παραμόρφωση κορυφής (apical sparing πρότυπο) στη μελέτη strain.3 Επίσης, η μαγνητική τομογραφία καρδιάς με τη δυνατότητα ιστικού χαρακτηρισμού, μπορεί να θέσει τη διάγνωση της καρδιακής αμυλοείδωσης κυρίως με βάση τις λίαν αυξημένες τιμές native T1 / κλάσματος εξωκυττάριου όγκου (ECV), αλλά και τη χαρακτηριστική διάχυτη καθυστερημένη υπενδοκάρδια ή/και διατοιχωματική ενίσχυση σήματος γαδολινίου στο μυοκάρδιο της αριστερής κοιλίας.3,4 Στο σπινθηρογράφημα οστών με ιχνηθέτες με βάση το Tc99m (DPD, PYP ή HMDP) η παρουσία ATTR οδηγεί στην ισχυρή πρόσδεση του ιχνηθέτη με τα ινίδια αμυλοειδούς στο μυοκάρδιο με αποτέλεσμα την αυξημένη ένταση σήματος στην περιοχή του καρδιακού μυός σε σχέση με τον αντίπλευρο ημιθωράκιο στις καθυστερημένες λήψεις (π.χ. στις 3 ώρες μετά τη χορήγηση του ιχνηθέτη).
Πολύτιμο εργαλείο για την ταυτοποίηση της νόσου και για την απόφαση για την καταλληλότερη αγωγή είναι ο γενετικός έλεγχος στο γονίδιο TTR. Η λειτουργία της ειδικής Μονάδας Κληρονομικών Καρδιαγγειακών Νοσημάτων (EKKAN) του Παν. Αθηνών εξυπηρετεί ακριβώς αυτό το σκοπό. Μια ομάδα ειδικά καταρτισμένων επιστημόνων παρέχει εξειδικευμένη ιατρική φροντίδα, δωρεάν γενετικό έλεγχο για την ATTR και τη συνολική υποστήριξη και συμβουλευτική των ασθενών και των οικογενειών με σπάνια νοσήματα όπως η αμυλοείδωση.

Επιθετικών ευρημάτων, η επιβεβαίωση με τομογραφικές λήψεις SPECT της καθήλωσης του ιχνηθέτη στο μυοκάρδιο, θέτει με αξιοπιστία τη διάγνωση της ATTR.5 Ιδιαίτερη προσοχή χρειάζεται για να αποκλειστεί φυσικά η περίπτωση του θετικού σπινθηρογραφήματος λόγω AL αμυλοείδωσης, οπότε επί θετικού σπινθηρογραφήματος οστών είναι απαραίτητος ο αποκλεισμός της αιματολογικής κακοήθειας.
Σήμερα, υπάρχουν διαθέσιμες θεραπείες, γι’ αυτό και η έγκαιρη διάγνωση είναι πολύ σημαντική. Στην «γεροντική» αμυλοείδωση από τρανσθυρετίνη ένα πολύ αποτελεσματικό φάρμακο είναι το tafamidis που σταθεροποιεί το μόριο της τρανσθυρετίνης. Η σταθεροποίηση αυτή του μορίου της τρανσθυρετίνης από το tafamidis οδηγεί σε σταθεροποιήση της λειτουργίας των οργάνων και βελτιώνει τα συμπτώματα της νόσου και την ποιότητα ζωής των ασθενών με μυοκαρδιοπάθεια ATTR. Η καθυστέρηση της προόδου της νόσου έχει ως αποτέλεσμα τη βελτίωση της πρόγνωσης και την παράταση του προσδόκιμου επιβίωσης των ασθενών με ATTR.6 Σε κάθε περίπτωση ασθενούς με ATTR (ανεξάρτητα από την ηλικία του) είναι επιβεβλημένος ο γενετικός έλεγχος. Σε περιπτώσεις οικογενούς αμυλοείδωσης λόγω μεταλλάξεων στο TTR γονίδιο, υπάρχει επίσης η δυνατότητα θεραπείας με μόρια που προκαλούν την ενδοκυττάρια σίγαση του γονιδίου TTR, όπως το patisiran. Αρκετές νέες ενώσεις βρίσκονται υπό πειραματική ανάπτυξη, συμπεριλαμβανομένων παραγόντων που κατευθύνονται στην απομάκρυνση των αμυλοειδών ινιδίων. Συμπερασματικά, ο έλεγχος για ATTR θα πρέπει να πραγματοποιείται συστηματικά σε όλους τους ασθενείς με υψηλή κλινική υποψία όπως υπερτροφία της αριστερής κοιλίας, HFpEF ή στένωση αορτικής βαλβίδας σε συνδυασμό με εξωκαρδιακά ευρήματα (red flags) δηλωτικά ATTR, (ειδικά ηλικιωμένους), ακόμα και σε ασθενείς με υπερτροφική μυοκαρδιοπάθεια χωρίς τα τυπικά ηλεκτροκαρδιογραφικά ευρήματα.1 Η καρδιακή απεικόνιση, συμπεριλαμβανομένης της χρήσης μαγνητικής τομογραφίας καρδιάς είναι πολύτιμη στη διάγνωση της νόσου ATTR, αλλά και στην παρακολούθηση της εξέλιξης της καρδιακής βλάβης και της ανταπόκρισης στη θεραπεία. Πολύτιμο εργαλείο για την ταυτοποίηση της νόσου και για την απόφαση για την καταλληλότερη αγωγή είναι ο γενετικός έλεγχος στο γονίδιο TTR. Η λειτουργία της ειδικής Μονάδας Κληρονομικών Καρδιαγγειακών Νοσημάτων (EKKAN) του Πανεπιστημίου Αθηνών (www.ekkan.gr) εξυπηρετεί ακριβώς αυτό το σκοπό. Μια ομάδα ειδικά καταρτισμένων επιστημόνων παρέχει εξειδικευμένη ιατρική φροντίδα, δωρεάν γενετικό έλεγχο για την ATTR και τη συνολική υποστήριξη και συμβουλευτική των ασθενών και των οικογενειών με σπάνια νοσήματα όπως η αμυλοείδωση.
ΒΙΒΛΙΟΓΡΑΦΊΑ